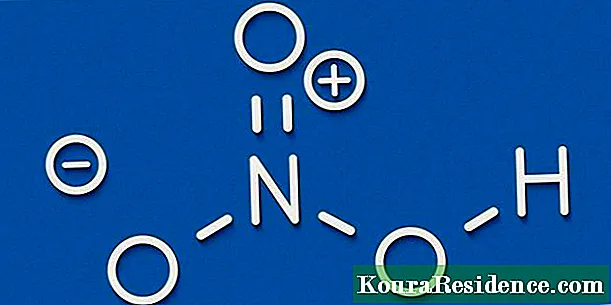
වල අණු සෑදීම සඳහා රසායනික සංයෝග, විවිධ ද්රව්ය හෝ මූලද්රව්යයන්ගේ පරමාණු ස්ථාවර ආකාරයකින් එකිනෙකා සමඟ සම්බන්ධ විය යුතුය, සහ අප දන්නා පරිදි ඉලෙක්ට්රෝන වලාකුළකින් වට වී ඇති ධන ආරෝපිත න්යෂ්ටියකින් සමන්විත සෑම පරමාණුවකම ඇති ව් යුහාත්මක ලක්ෂණ අනුව මෙය විවිධාකාරයෙන් සිදුවිය හැකිය.
ඉලෙක්ට්රෝන negativeණ ආරෝපිත වන අතර න්යෂ්ටියට සමීපව පවතින නිසා විද්යුත් චුම්භක බලය ඔවුන් ආකර්ෂණය කරයි. ඉලෙක්ට්රෝනයක් න්යෂ්ටියට සමීප වන තරමට එය මුදා හැරීමට අවශ්ය ශක්තිය වැඩි වේ.
නමුත් සියලුම මූලද්රව්ය එක සමාන නොවේ: සමහර ඒවා වලාවෙන් පිටත ඉලෙක්ට්රෝන අහිමි වීමේ ප්රවනතාවයක් ඇත (අඩු අයනීකරණ ශක්තියක් ඇති මූලද්රව්ය), අනෙක් ඒවා ඒවා ග්රහණය කර ගැනීමට උත්සාහ කරති (ඉහළ ඉලෙක්ට්රෝන සම්බන්ධතාවයක් ඇති මූලද්රව්ය). මෙය සිදු වන නිසා ලුවිස් ඔක්ටේට් නීතියට අනුව, ස්ථායිතාව, අවම වශයෙන් බොහෝ අවස්ථාවලදී අවම වශයෙන් කවචයේ හෝ කක්ෂයේ ඉලෙක්ට්රෝන 8 ක් තිබීම හා සම්බන්ධ වේ.
එහෙනම් කොහොමද ඉලෙක්ට්රෝන නැතිවීම හෝ ලැබීම විය හැකිය, ප්රතිවිරුද්ධ ආරෝපණ අයන සෑදිය හැකි අතර, ප්රතිවිරුද්ධ ආරෝපණ අයන අතර විද්යුත් ස්ථිතික ආකර්ෂණය නිසා මේවා එකතු වී සරල රසායනික සංයෝග සෑදෙන අතර එමඟින් එක් මූලද්රව්යයක් ඉලෙක්ට්රෝන ලබා දුන් අතර අනෙකට ඒවා ලැබුණි. මෙය සිදුවිය හැකි වන පරිදි සහ අ අයනික බන්ධනය අවම වශයෙන් 1.7 ට සම්බන්ධ වූ මූලද්රව්ය අතර විද්යුත් gaණතාවයේ වෙනසක් හෝ ඩෙල්ටාවක් තිබීම අවශ්ය වේ.
එම අයනික බන්ධනය සාමාන්යයෙන් ලෝහමය සංයෝගයක් සහ ලෝහමය නොවන එකක් අතර සිදු වේ: ලෝහ පරමාණුව ඉලෙක්ට්රෝන එකක් හෝ කිහිපයක් අත්හරින අතර එමඟින් ධන ආරෝපිත අයන (කැටායන) සෑදෙන අතර ඒවා නොවන වානේ ලබාගෙන lyණ ආරෝපිත අංශුවක් බවට පත් වේ. ක්ෂාර සහ ක්ෂාරීය පස් ලෝහ යනු කැටායන සෑදීම සඳහා මූලද්රව්යයන් වන අතර හැලජන් සහ ඔක්සිජන් සාමාන්යයෙන් ඇනායන වේ.
සාමාන්යයෙන්, අයනික බන්ධනයෙන් සෑදෙන සංයෝග වේ කාමර උෂ්ණත්වයේ සහ ඉහළ ද්රවාංකයේ ඇති ද්රව්ය ජලයේ ද්රාව්ය වේ. විසඳුමේදී ඒවා ඉතා ය හොඳ විදුලි සන්නායකමන්ද ඒවා ප්රබල ඉලෙක්ට්රෝලයිට් ය. අයනික ඝන ද් රව් යයක දැලිස් ශක්තිය එම ඝණයේ අයන අතර ආකර්ෂණීය බලය සලකුනු කරයි.
එය ඔබට සේවය කළ හැකිය:
- සහසංයුජ බන්ධන සඳහා උදාහරණ
- මැග්නීසියම් ඔක්සයිඩ් (එම්ජීඕ)
- තඹ සල්ෆේට් (CuSO4)
- පොටෑසියම් අයඩයිඩ් (KI)
- සින්ක් හයිඩ්රොක්සයිඩ් (Zn (OH) 2)
- සෝඩියම් ක්ලෝරයිඩ් (NaCl)
- රිදී නයිට්රේට් (AgNO3)
- ලිතියම් ෆ්ලෝරයිඩ් (LiF)
- මැග්නීසියම් ක්ලෝරයිඩ් (MgCl2)
- පොටෑසියම් හයිඩ්රොක්සයිඩ් (KOH)
- කැල්සියම් නයිට්රේට් (Ca (NO3) 2)
- කැල්සියම් පොස්පේට් (Ca3 (PO4) 2)
- පොටෑසියම් ඩයික්රොමේට් (K2Cr2O7)
- ඩිසෝඩියම් පොස්පේට් (Na2HPO4)
- යකඩ සල්ෆයිඩ් (Fe2S3)
- පොටෑසියම් බ්රෝමයිඩ් (කේබීආර්)
- කැල්සියම් කාබනේට් (CaCO3)
- සෝඩියම් හයිපොක්ලෝරයිට් (NaClO)
- පොටෑසියම් සල්ෆේට් (K2SO4)
- මැංගනීස් ක්ලෝරයිඩ් (MnCl2)